Brustkrebs Therapie, Brustkrebs Behandlung
Brustkrebs Therapie, Metastasen Behandlung, Hormontherapie, Bestrahlung, Mistel Therapie, Heilungschansen, Nebenwirkungen, Nachsorge
In Deutschland gibt es zertifizierte Brustzentren an Krankenhäusern und ein Disease-Management-Programm für Brustkrebs, an dem sich auch niedergelassene Ärzte beteiligen können. Die gemeinsame Leitlinie der Stufe S3 gilt als die Orientierung zur Behandlung von Brustkrebs. Diese Leitlinie wird regelmäßig aktualisiert, zuletzt im Dezember 2017, Version 4.0. => S3 Leitlinien Brustkrebs
Außer vielen Änderungen im Bezug auf Behandlung und Diagnostik, sind in der Leitlinen neue Kapitel hinzugekommen:
- Kapitel 4.7.6: Knochengerichtete Therapie
- Kapitel 4.7.7: Beeinflussbare Lebensstilfaktoren
- Kapitel 7: Mammakarzinom in Schwangerschaft und Stillzeit, Schwangerschaft nach Mammakarzinom, Fertilitätserhalt
- Kapitel 8: Mammakarzinom der älteren Patientin
- Kapitel 9: Mammakarzinom des Mannes
Die Strategie zur Brustkrebsbehandlung wird meist im Rahmen einer Tumorkonferenz geplant, an der sich Gynäkologen, internistische Onkologen, Radiologen, Strahlentherapeuten und Pathologen beteiligen. Die Einbindung der Patientin in die Entscheidungsfindung ist wie bei jeder eingreifenden medizinischen Maßnahme von großer Bedeutung.
Die Therapie der Brustkrebserkrankung soll im Frühstadium eine Heilung, beim metastasen brustkrebseine Lebenszeitverlängerung und im Spätstadium eine Linderung der Krankheitsbeschwerden erreichen.
Wichtig!: Das Risiko für ein Brustkrebs-Rezidiv besteht noch viele Jahre nach Abschluss der Therapie. Laut New England Journal of Medicine noch nach 20 Jahren nach der Diagnose eines Mammakarzinoms besteht die Gefahr für den Rückkehr der Erkrankung in Form von Metastasen.
Bei der Wahl der konkreten Therapie steht die Erhaltung der Lebensqualität im Vordergrund. Darum wird neben den Klassifikationen des Tumors auch die körperliche, psychosoziale und emotionale Situation der Patientin berücksichtigt.
Eine „Standardtherapie“ gibt es nicht, die Berücksichtigung aller verschiedenen Faktoren führt zu einer individuellen Anpassung der Therapie an die Krankheit und an die jeweilige Patientin.
Die multimodale Therapie von Brustkrebs
Die multimodale Therapie ist eine Therapiemethode, in der nacheinander (sequenziell) verschiedene Behandlungen eingesetzt werden. Dadurch werden die Therapieergebnisse optimiert.
Die Individualisierung der Behandlungsstrategie wird auf der Grundlage patienten- und tumorabhängiger Faktoren durchgeführt.
Bei der multimodalen Therapie von Mammakarzinom werden in meisten Fällen folgende Behandlungen durchgeführt:
Operation, Bestrahlung, Hormontherapie und Chemotherapie.
Zusätzliche Maßnahmen vor einer Operation werden als neoadjuvant bezeichnet, nach einer Operation nennt man sie adjuvant.
Brustkrebs kann sich sehr schnell im Körper ausbreiten und wird schon in frühen Stadien mit einer systemischen (im ganzen Körper wirksamen) Therapie behandelt. Diese „Fisher-Doktrin“ (benannt nach dem amerikanischen Chirurgen Bernard Fisher) ist die Grundlage der Chemo- und Hormontherapie beim Brustkrebs.
Die Operation
Bei der Diagnose Brustkrebs ist in den meisten Fällen ein chirurgischer Eingriff notwendig. Dabei spielt die Größe des Tumors bei der Wahl der Operationstechnik eine wesentliche Rolle.
Grundsätzlich besteht bei einer Brustkrebs-Operation keine Gefahr der Verschleppung von Tumorzellen.
Jedoch zahlreiche Untersuchungen deuteten Darauf hin, dass die Operation einen ungünstigen Einfluss auf den Verlauf der Brustkrebserkrankung haben kann.
Es gibt Hinweise darauf, dass diese ungünstigen Folgen der Operation durch den Einsatz bestimmter Entzündungshemmer während der Operation diese Tumorreaktionen unterbinden kann, so dass die mögliche Streuung und Aktivierung von Krebsstammzellen verhindern werden können.
Die Wissenschaftler vermuten, dass die Kombination eines Betablockers und eines Antiphlogistikums eine geeignete Strategie sein könnte das erhöhte Metastasierungs-Risiko zu senken. Frauen profitieren möglicherweise davon, wenn sie vor einer anstehenden Brustkrebs-Operation eine Begleitmedikation mit einem Betablocker und einem COX-Hemmer beginnen und diese auch nach dem Eingriff noch einige Tage anwenden.
Brusterhaltene Therapie
Bei brusterhaltenen Operation schneiden die Operateure lediglich das veränderte Gewebe mit etwas gesundem Gewebe aus der Brust. Nach dem Eingriff ist es ratsam eine Bestrahlung der Brust, wegen einem Rückfall im verbliebenen Gewebe, durchzuführen. Das Gewebe wird auf Zellveränderungen untersucht.
Die brusterhaltende Therapie gilt aktuell als Maßstab bei Mammakarzinom.
Wichtig ist den ganzen Tumor zu entfernen, eine R0-Resektion (kein Tumorgewebe am Schnittrand) zu erreichen, um das Risiko für Lokalrezidiv zu minimieren.
Für die folgende adjuvante Strahlentherapie und die medikamentöse Therapie ist die korrekte Kennzeichnung des Operationsfeldes durch den Operateur (eine Clipmarkierung des Tumors).
Amputation, Mastektomie
Bei der Mastektomie wird das ganze Brustdrüsengewebe entfernt mit der darüber liegenden Haut, mit dem Bindegewebe des Brustmuskels (Faszie), Brustwarze und Warzenhof.
Der Muskel bleibt erhalten.
Dasentfernte Gewebe wird genau untersucht um das Erkrankungsstadium festzustellen.
Gründe, für die Mastektomie sind:
- An mehreren Stelle wachsen Tumore
- Keine sichere Entfernung wegen der Lage und die Größe des Tumors
- Die Brust ist entzündet
- Eine Nachbestrahlung ist unmöglich oder wird von der Patientin nicht toleriert
- Der Tumor konnte trotz Nachoperation nicht vollständig entfernt werden.
Bei einer Amputation der Brust ist in der Regel keine Bestrahlung nötig. Nach Absprache mit dem Arzt kann während einer Amputation schon mit dem Wiederaufbau der Brust begonnen werden.
Lymphknotenentfernung aus der Achsel
Da die Brustzellen über die Lymphknoten in den Körper streuen können, werden die Wächterlymphknotenen der unteren und mittleren Achselhöhle mittels einer Sentinel-Node-Biopsie untersucht.
Sentinel Lymphknoten Biopsie:
Bei der Biopsie wird der sogenannte Wächter-Lymphknoten entfernt. Der erste oder die ersten ableitenden Lymphknoten werden über eine Markierungstechnik mit einer schwach radioaktiven Substanz oder eine blaugefärbte Lösung identifiziert und entfernt.
Wenn die Lymphknoten tumorfrei sind, wird eine Operation der Achselhöhle nur in den seltenen Fällen durchgeführt.
Wenn die Wächterlymphknotenen Tumorzellen enthalten, kann es nötig sein, eine ausreichende Zahl von Lymphknoten, mindestens zehn, in der Achselhöhle zu entfernen (Lymphadenektomie oder Axilladissektion).
War der Tumor nicht sehr groß ist (pT1, pT2, klinisch N0) und sind nur ein bis zwei Lymphknoten befallen, kann eventuell auf die Achselhöhlenoperation verzichtet werden.
Lymphstau. Durch dieie operative Entfernung der Lymphknoten können ein Lymphstau sowie Lymphödeme auftreten.
Je mehr Lymphknoten entfernt bzw. bestrahlt wurden, desto steigt das Risiko für Lymphstau.
Ein Lymphödem entwickelt dich bei 25 bis 30 Prozent der Frauen nach Entfernung der Lymphknoten.
Wurden weniger als drei Knoten entfernt, liegt das Risiko bei zehn Prozent.
Ein Lymphstau kann direkt nach der OP auftreten, aber auch erst in einigen Monaten oder sogar Jahren.
Wenn sich ein Ödem entwickelt, erhalten die Frauen erst einmal eine tägliche Lymphdrainage. Eine Lymph-Therapeutin streicht mit speziellen Griffen gestaute Flüssigkeit am Arm stufenweise nach oben und verteilt sie über verbindende Lymphbahnen in Richtung der gesunden Körperseite.
Damit die positive Wirkung von Lymphdrainage anhält, muss die Therapeutin einen Kompressionsverband aus mehreren Schichten anlegen.
Mögliche Operationsfolgen: Ein Serom in der Achselhöhle: In der Wundhöhle sammelt sich Wundflüssigkeit, das man meistens mit einer Spritze abziehen kann. Nervenstränge können durchtrennt werden. Es kann zu Taubheitsgefühlen im Schulter –Armbereich, auch durch die Narbenbildung zu einer eingeschränkten Beweglichkeit im betroffenen Schultergelenk, kommen.
Brustaufbau nach Amputation, Rekonstruktion mit Eigengewebe, Silikonprothesen, Einlagen
Wird die Brust nicht wieder aufgebaut, kann es zu einer Fehlbelastung der Schulter oder des Rückens kommen.
Schon im Krankenhaus erhalten betroffene Frauen Erstversorgungs-BHs sowie Brustprothesen. Diese Einlagen sind weich und leicht, um die Wundheilung nicht zu behindern und die Haut zu schonen.
Bei der Rekonstruktion Brustaufbaus gibt es mehrere Möglichkeiten, von Einsetzen gelgefüllter Silikonimplantate bis zu verschiedenen Verfahren der Brustrekonstruktion mit Eigengewebe. Auch eine Kombination beider Verfahren ist möglich. Die Brustwarze kann auch rekonstruiert werden.
Das Silikon hat die ähnliche Dichte wie Brustgewebe. Die Silikoneinsätze müssen regelmäßig kontrolliert werden.
Mehr über Brustaufbau: => brustaufbau-nach-brustentfernung
Bestrahlung, Strahlentherapie
Die Strahlentherapie wird grundsätzlich nach einer brusterhaltenden Therapie durchgeführt. Sie kann allein oder in Verbindung mit Chemotherapie durchgeführt werden.
Die Strahlentherapie hat die Heilung der Tumorerkrankung zum Ziel, kann aber sowohl bei einem bestehenden Tumor als auch vorbeugend durchgeführt werden, wenn befürchtet wird, dass z. B. im Operationsgebiet noch vereinzelte Tumorzellen zurückgeblieben sind.
Bei der Strahlentherapie kommen energiereiche (ionisierende) Strahlen zur Anwendung. Die Hauptwirkung besteht in der Hemmung der Zellteilung und Zerstörung der Krebszellen.
Die Strahlentherapie erfolgt meistens ambulant.
Wenn die Therapie im Anschluss an eine brusterhaltende Operation erfolgt, werden die Strahlenbehandlungen für fünf bis sechs Wochen an fünf Tagen in der Woche durchgeführt.
- Adjuvante Strahlentherapie wird nach der Brust-Operation durchgeführt, besonders wichtig ist sie nach einer brusterhaltenden Operation. Auch nach einer Mastektomie wird die Brustwand bei einigen Patientinnen bestrahlt, um das Risiko für Rückfall zu senken.
Die Bestrahlung soll in der Brust und dem umgebenden Gewebe verbliebene Tumorzellen vernichten. - Die Achselhöhle können bei Bedarf bestrahlt werden.
- Bei einer fortgeschrittenen Brustkrebserkrankung ist ebenfalls eine Bestrahlung möglich. Bei einem örtlichen Rückfall kann sie den Tumor in der Brust oder der Brustwand an der Ausbreitung hindern.
- Bestrahlung von Tumormetastasen, besonders die Bestrahlung von Knochenmetastasen wird oft durchgeführt.
Die Bestrahlung bei einer Adjuvante Strahlentherapie kann moderate Hypofraktionierung (verkürzte Bestrahlung) mit einer Gesamtdosis von etwa 40 Gy in circa 15–16 Fraktionen durchgeführt werden. Durch diese neue Form der Bestrahlung können die Dauer der Behandlung und die Nebenwirkungen reduziert werden.
Intraoperative Radiotherapie (IORT)
Schon seit 2002 werden an der Universitätsmedizin Mannheim intraoperative Bestrahlungen
während Brustkrebsoperationen mit dem INTRABEAM® System (arbeitet mit niederenergetischen
Röntgenstrahlen mit maximal 50 kV) erfolgreich durchgeführt. Inzwischen in mehr als 50 Brustzentren in Deutschland kann diese Therapieform eingesetzt werden. Diese mobile Bestrahlungseinheit besteht aus einer Miniaturröntgenquelle mit einer Sonde, an deren Ende kugelförmige Applikatoren angebracht werden können, einer Steuereinheit und einem Trägersystem, einer Art Stativ.
Während der Operation wird nach der vollständigen Entfernung des Tumorgewebes der passende kugelförmige Applikator (1,5 – 5 cm im Durchmesser je nach Größe des entfernten Präparats) in die Wundhöhle eingebracht und eine Einzeldosis von 20 Gray auf das Tumorbett , also das die Wundhöhle begrenzende Gewebe verabreicht. Dies dauert in Abhängigkeit von der Größe des verwendeten
Applikators etwa 20 – 50 Minuten.
Vorteile der IORT:
- Fehlende zeitliche Verzögerung zwischen Tumorentfernung und Beginn der Strahlentherapie
- Kein Risiko, das Tumorbett bei der Bestrahlung zu verfehlen („geographical miss“)
- Schonung der Haut und des umgebenden Gewebes (Herz, Lunge)
- Verkürzung/ggf. Wegfall der postoperativen Strahlentherapie
- Verbesserte Lebensqualität bei alleiniger IORT
- Weniger Brust /Arm-Symptome und Schmerzen
- das Risiko innerhalb von 5 Jahren ein Brustkrebsrezidiv zu erleiden nach einer brusterhaltenden Therapie mit IORT gefolgt von einer verkürzten externen Bestrahlung unter 2% liegt.
Nachteile der IORT
- Verlängerung der Operationszeit um ca. 20-30 Minuten
- Möglichkeit der Durchführung einer IORT hängt von der Tumorgröße und Lokalisation ab
- Begrenzte Datenlage im Vergleich zur externen Bestrahlung
- Investitionskosten
Bestrahlung bei Metastasenbildung:
Die Bestrahlung bei einer fortgeschrittenen Brustkrebserkrankung wird individuell an die Situation der Patientin angepasst. Wie die Bestrahlungsplanung abläuft, ob nur gezielt eine Metastase bestrahlt wird oder eine größere Körperregion, hängt von der Krankheitssituation ab. Auch die Strahlendosis passen die Radiologen an den Verlauf der Erkrankung an.
Nebenwirkungen der Bestrahlung:
Akute Schäden (innerhalb von 90 Tagen)
- Hautrötungen, sogenannte Erythem
- Braune Pigmentflecken
- Schuppige Haut
- Selten Brandblasen
- Schwellungen
- Spannungsgefühl
- Eventuell: müde, kraft, appetitlos, Übelkeit
Langzeitschäden der Bestrahlung:
- Die Haut ist empfindlicher
- Die Hautfarbe der bestrahlten Fläche ist anders als die Umgebung
- Mögliche Verhärtungen oder Vernarbungen möglich
- Mögliche Gewebeschäden der Lunge, Schilddrüse, Speiseröhre, Herz möglich
- Mögliche Funktionseinschränkungen
Spätschäden
Selten:
- Risiko für Lungen-Speiseröhrenkrebs steigt
- Risiko für ein Angiosarkom, für ein bösartiger Tumor des Stütz- und Bindegewebes
Brachytherapie
Die Brachytherapie ist eine spezielle Form der Strahlentherapie (= sog. interstitielle Brachytherapie).
Sie wird zur Nachbehandlung der operierten Brust eingesetzt und ermöglicht es, die erkrankte Stelle so präzise zu bestrahlen, dass benachbarte Gewebe und Organe nicht belastet werden.
Bei dieser Therapie werden der Patientin in Kurznarkose dünne Plastikkatheter in den Bereich der operierten Brust eingebracht. Dann wird ein Strahlenträger in diese Röhrchen transportiert, wobei die Strahlenexposition nur einige Minuten pro Tag dauert.
Diese Behandlung wird stationär durchgeführt und ist meistens nach fünf Tagen abgeschlossen.
Nebenwirkungen der Metastasenbestrahlung in Knochen, die viel Knochenmark enthalten.
Es kann passieren, dass weniger rote und weiße Blutkörperchen und Blutplättchen gebildet werden.
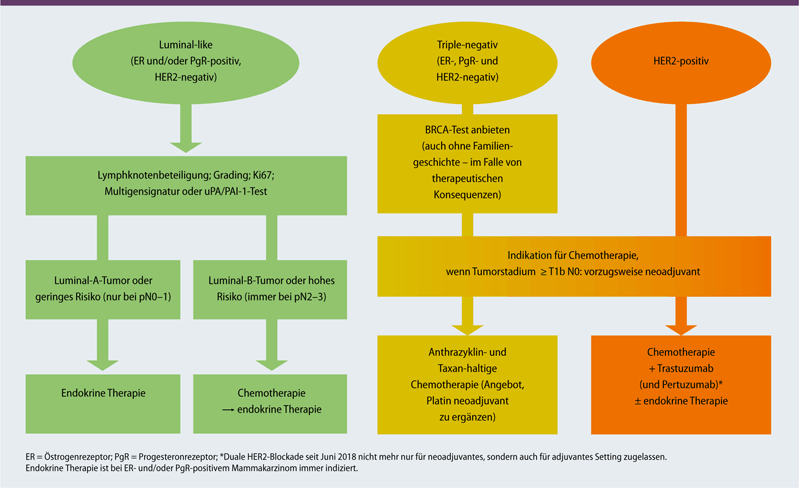
Adjuvante systemische Therapie, wahl der Therapie
Bei einer adjuvanten Systemtherapie (nach einer Erstbehandlung wie Operation) sollen bereits vorhandene Mikrometastasen behandelt werden, um das Risiko eines Tumorrezidivs als auch Sterberisiko zu senken.
Bild Quelle: www.springermedizin.de/
Für die Wahl der Therapie werden verschiedene Faktoren berücksichtigt, wie Aggressivitätsgrad des Tumors, das Vorkommen spezifischer Rezeptoren auf der Oberfläche der Tumorzelle, Rezeptor für den „human epidermal growth factor“ (HER2).
Abkürzungen: ER Östrogenrezeptor; PR Progesteronrezeptor.
Mit Hilfe folgender Angaben kann der behandelnde Gynäkologe festlegen, welche Art der Therapie in dem individuellen Fall der Patientin gewählt werden sollte:
| Intrinsischer Subtyp |
Rezeptor expression |
Proliferations index |
Therapie empfehlung |
| Luminal A | ER+/ PR+/ HER2- | niedrig | Hormontherapie |
| Luminal B | ER+/PR+/ HER2- | hoch | Chemotherapie+ Hormontherapie |
| Luminal B/ HER2 positiv |
ER+/ PR+/ HER2+ | unabhängig | Chemotherapie+ Antikörpertherapie+ Hormontherapie |
| HER2 positiv | ER-/ PR-/ HER2+ | unabhängig | Chemotherapie+ Antikörpertherapie |
| Triple negativ | ER-/ PR-/ HER2- | unabhängig | Chemotherapie |
Genauere Beschreibung/Erklärung für die in der Tabelle benutzte Begriffe finden Sie auf der Seite: => Klassifikation Brustkrebs
Hormonentzugstherapie, Antihormontherapie
Bei 70% der an Brustkrebs erkrankten Frauen ist das Wachstum der Krebszellen vom Hormon Östrogen abhängig.
Die Brustkrebs-Zellen dank spezieller Rezeptoren reagieren auf das Hormon Östrogen. Bindet sich das Hormon an diese Rezeptoren, kann dies das Tumorwachstum provozieren.
In diesem Fall wird meistens eine Anti-Hormontherapie eingesetzt. In Betracht kommen hier Östrogenrezeptorantagonisten wie Tamoxifen und/oder Aromatashemmern.
Einen Hormonrezeptorstatus kann man durch Tumorgewebeproben erstellen.
Wenn die Tumorzellen Rezeptoren für Östrogen oder Progesteron haben, also „Hormonrezeptor positiv“ (es reicht auf unter 10 % der Tumorzellen), es sollte eine Antihormontherapie durchgeführt werden.
- Sie soll die Bildung und Wirkung des Östrogens blockieren
- Das Wachstum hormonempfindlicher Tumorzellen stoppen
- Ein weiteres Wachstum verhindern
- Nach einer Operation einen Rückfall verhindern
Bei Patientin vor den Wechseljahren wird in aller Regel eine Tamoxifentherapie verschrieben. Nach den Wechseljahren wird neben Tamoxifen auch ein sogenannter Aromatasehemmer (z.B. Anastrozol) verschrieben, der die Östrogenproduktion vor allem im Fett- und Nebennierengewebe unterdrücken soll.
Medikamente und deren Wirkung:
- GHRH-Analoga (Medikamente, die einem Steuerungshormon des Hormonkreislaufs ähnlich sind und bei Patientinnen vor der Menopause eingesetzt werden, um die körpereigene Aktivierung der Hormonbildung zu unterdrücken). GnRH-Analoga bedeutet „Geschlechtshormone freisetzendes Hormon“ Wiederum bedeutet, dies ist ein steuerndes Hormon, das im Gehirn im Hypothalamus gebildet wird. Es regelt den Stoffwechsel der Sexualhormone.
- Tamoxifen und Fulvestrant als Östrogenrezeptorblocker
- sog. Aromatasehemmer, die die Bildung von Östrogenen hemmen
Tamoxifen, Anti-Östrogen
Wird angewendet nach Op und bei fortgeschrittenem Brustkrebs. Es wird in Tablettenform eingenommen.
Tamoxifen verhindert, dass Östrogen an die Tumorsrezeptoren andocken und blockiert damit die Wirkung der Geschlechtshormone. Dadurch wachsen die östrogenabhängigen Krebszellen viel langsamer.
Die Tamoxifen blockiert die Tumorzellen auch bei älteren Frauen. Östrogen wird im Körper weiterhin in geringerer Mengen freigesetzt.
Bei Brustkrebsfrühstadium nach einer großzügigen OP profitieren Patientinensie besonders von der Kombination aus Bestrahlung plus Tamoxifen. Die Lokalrezidivrate wird damit drastisch reduziert.
Tamoxifen ist am wirksamsten bei Frauen in einem noch frühen Stadium, die bereits eine Tumor-Operation hinter sich haben, bestrahlt wurden oder bei denen eine Chemotherapie durchgeführt wurde. Tamoxifen soll in all diesen Fällen ein Wiederaufflackern der Krankheit verhindern.
Nach Bericht von Professor Dowsett und seinem Team vom Institut für Krebsforschung (ICR) in Großbritannien, bewirkt die Einnahme von Tamoxifen über einen Zeitraum von fünf Jahren eine Minimierung des Sterberisikos an Brustkrebs um 30%.
Die aktuellen Studien legen nahe, dass die Aromatase-Hemmer wesentlich wirksamer arbeiten als Tamoxifen. Das Sterberisiko in den beschriebenen Fällen sank um 40% innerhalb der zehn Jahre nach der ersten Behandlung.
Nebenwirkung von Tamoxifen:
- Knochenschmerzen bei Therapiebeginn
- Hitzewallungen
- Zyklusveränderungen
- Ausbleiben der Menstruation
- Sekretausfluß der Scheide
- Juckende Scheide
- Blutbildveränderung
- Benommenheit
- Kopfschmerzen
- Übelkeit
Tamoxifen wird in Tablettenform verabreicht. Es ist möglich die Tamoxifen Behandlung mit anderen Therapien, je nach Tumorbefall, kombinieren. Ob eine oder mehrere ergänzenden Therapien sinnvoll sind, hängt vom den Tumoreigenschaften, dem Alter und der hormonellen Situation einer Frau ab.
Aromatasehemmer
Bei Frauen nach den Wechseljahren produzieren die Eierstöcke kein Östrogen mehr. Im Körper wird jedoch weiterhin in geringerer Mengen Östrogen freigesetzt: das Enzym Aromatase produziert es in anderen Geweben (hauptsächlich Fettgewebe) aus Östrogenvorstufen, die in der Nebennierenrinde gebildet werden.
Die Aromatase-Hemmer senken das Östrogen-Niveau, indem sie die Entstehung des Enzyms Aromatase verhindern. Dieses Enzym findet sich überwiegend in Fettgewebe. Es ist in der Lage, andere Hormone in Östrogen umzuwandeln. Je weniger Östrogen sich im Organismus befindet, desto weniger Rezeptoren in den Krebszellen werden angesprochen.
Medikamente Anastrozol, Letrozol und Exemestan sind Aromatasehemmer, die Wirkstoffe sind bei Allen gleich.
Leider rund 25 Prozent der Frauen legen die Pillen für Antihormontherapie zu früh zur Seite oder beginnen die Therapie erst gar nicht. Der Grund seien die Nebenwirkungen, berichten Forscher der University of Michigan Comprehensive Cancer Center.
Die Forscher befragten 743 Frauen mit hormonempfindlichem Brustkrebs neun Monate und vier Jahre nach der Diagnose Brustkrebs. Elf Prozent hatten die Therapie mit Tamoxifen oder einem Aromatasehemmer erst gar nicht begonnen. 15 Prozent stoppten die Therapie vor den empfohlenen fünf Jahren.
Der häufigste Grund für den Medikamentenstopp waren die Nebenwirkungen der endokrinen Therapie. Viele Frauen erlebten heftige Wechseljahressymptome wie Hitzewallungen oder vaginale Trockenheit. Und beide Typen von Medikamenten, vor allem aber Aromatasehemmer, führten zu Gelenkschmerzen. Die Hochrisikopatientinnen sollen die Tabletten ca. zehn Jahre einnehmen.
Nebenwirkungen von Aromatasehemmer:
- Hitzewallungen und Errötung (Flushes)
- Müdigkeit
- Kopfschmerzen
- Übelkeit
- Depressionen
- Schlafstörungen
- Verschlechterung der Cholesterinwerte
- Osteoporose
Schmerztherapie mit Medikamenten bei Krebs
Beim Fortschreiten der Krebserkrankung kommt oft zu starken Schmerzen.
Die Schmerzen stören den Schlaf, mindern den Appetit, verhindern körperliche und geistige Aktivitäten, führen zu sozialem Rückzug, zu psychischer und physischer Erschöpfung, zur depressiven Stimmung.
Ausführliche Informationen über medikamentöse Behandlung von Schmerzen bei Krebs finden Sie hier: => Schmerztherapie mit Medikamenten
Chemotherapie
Bei aggressivem Brustkrebs (tripel-negativ, HER2-positiv) sollte man nach Mammakarzinom-Op mit der Chemotherapie nicht länger als 60 Tageo warten, da bei spätem Beginn die Überlebenschancen senken dramatisch (Quelle: springermedizin.de).
Bei der Entscheidung, ob eine Chemotherapie nötig ist oder nicht kann der uPA/PAI-1-Test helfen.
Bei einer Chemotherapie gegen Brustkrebs werden in der Regel verschiedene Medikamente mit unterschiedlichen Wirkmechanismen kombiniert.
Chemotherapie bei Brustkrebs: => auf der Seite : => Chemotherapie
Bisphosphonate und Denosumab
Bei Knochenmetastasen, bei Rezidiven (wiederkehrendem) Krebs, bei Osteoporose (Nebenwirkung der Hormonblockade) werden Medikamente eingesetzt, die das Wachstum des Tumors verlangsamen und Schmerzen lindern. Das sind Medikamente aus der Gruppe der Bisphosphonate und seit neuem Denosumab (XGeva), das noch besser wirkt.
Bisphosphonate (z.B. Zometa) werden monatlich als Infusion eingesetzt. XGeva als Spritze, subkutan in den Bauch.
Darüber hinaus sind Bisphosphonate und Denosumab auch zur Vorbeugung und Behandlung von Osteoporose zugelassen. Wichtig ist die gleichzeitige tägliche Einnahme von 1g Calcium mit Vitamin D.
Immuntherapie Brustkrebs, Antikörpertherapie, Herceptin, Lapatinib
Der gentechnisch hergestellte monoklonale Anti-körper Herceptin (Trastuzumab) ist zur Immuntherapie des metastasierten Mammakarzinoms zugelassen.
Antikörper-Medikamente wirken vergleichbar den natürlichen Abwehrstoffen und deshalb auch als Immuntherapie bezeichnet werden. Es handelt sich dabei um eine passive Immunisierung.
Mehr über Krebs Immuntherapie finden Sie hier: => Krebs Immuntherapie
Herceptin eignet sich nur für die Patientinnen, auf deren Tumoren das “Her2”-Protein überdurchschnittlich häufig vorkommt.
Bei ca. 10 % aller Brustkrebstumoren bilden sich Wachstumsrezeptoren (HER-2/neu-Rezeptoren) auf der Oberfläche. Gegen diese Rezeptoren wurde ein Antikörper mit dem Handelsnamen Herceptin® entwickelt. Eine weitere Möglichkeit ist Lapatinib, der die Stoffwechselwege in der Tumorzelle hemmt, die über den Her-2-neu-Rezeptor aktiviert werden. Herceptin wird adjuvant nach Abschluss der Chemotherapie für ein Jahr gegeben.
“Trastuzumab” ist offenbar in der Lage, die Her2-Rezeptoren zu besetzen und auf diese Weise ihre wachstumsfördernden Impulse zu unterdrücken. Auf Grund der Rezeptorblockade verlangsamt sich das Wachstum von Krebsherden für eine gewisse Zeit. In Kombination mit einer Chemotherapie, insbesondere wenn dabei so genannte Taxane verwendet werden, ist Herceptin noch effektiver: Frauen, die bereits Tochtergeschwülste (Metastasen) hatten, blieben bei dieser Therapie einige Monate länger von neuen Metastasen verschont als Frauen, die nur eine Chemotherapie erhielten.
Auch Lapatinib wird mit einem Chemotherapiemittel kombiniert.
Herceptin kann den Herzmuskel schädigen und sollte deshalb nicht mit den Anthracyclinen (Chemotherapiemittel, die dies ebenfalls tun) gleichzeitig gegeben werden. Unter Herceptin sollte alle drei Monate mit Ultraschall die Pumpkraft des Herzens überprüft werden. Stellt sich eine beginnende Schwäche dar, so muss das Medikament abgesetzt werden, dann kommt es zu einer vollständigen Erholung.
Ob Lapatinib die gleichen Probleme hervorruft, ist noch nicht genau bekannt. Auf jeden Fall ist auch hier Vorsicht geboten. Lapatinib kommt zunächst bei Patientinnen mit Metastasen zum Einsatz, die unter Herceptin weiter wachsen, also resistent werden.
Lapatinib eignet sich auch für die Therapie von Hirnmetastasen, da das Molekül so klein ist, dass es durch die sog. Blut-Hirn-Schranke in das Gehirn gelangt. Auch Lapatinib wird mit einem Chemotherapiemittel kombiniert.
Impfstoff gegen Brustkrebs
Der Impfstoff NeuVax® besteht aus dem Peptid E75.
Die Idee hinter NeuVax besteht darin, das Immunsystem gegen HER zu sensibilisieren, damit T-Zellen einen Angriff auf den Tumor starten.
Um diese Wirkung zu verstärken, enthält der Impfstoff noch den Wachstumsfaktor GM-CSD. Die Firma Apthera aus Scottsdale/Arizona evaluiert die Vakzine derzeit beim Mammakarzinom und beim Prostatakarzinom
NeuVax ist derzeit in einer internationalen Phase-3 vorhanden. Es laufen auch Studien mit NeuVax in Kombination mit Trastuzumab (Herceptin®)
Ein neuer Impfstoff für Immuntherapie in der Entwicklung ist GP2, hilft gegen Rückfälle bei Patienten mit HER2-positivem Brustkrebs.
Zielgerichtete Therapie
Zielgerichtete Wirkstoffe gegen Brustkrebs blockieren gezielt Vorgänge in Krebszellen, die für das Wachstum von Tumorgewebe wichtig sind. Die Zielstrukturen der Medikamente bezeichnen Fachleute auch als “Targets” (von englisch: target = Ziel). Deshalb wird diese Form der Therapie auch “targeted therapy” und auf Deutsch “zielgerichtete Therapie” genannt. Seltener gebräuchlich ist die Bezeichnung “molekulare” oder “molekularbiologische” Therapie.
In Deutschland sind für die Behandlung von Brustkrebs derzeit vier zielgerichtete Wirkstoffe als Arzneimittel zugelassen. Fast immer wird die Behandlung mit anderen Verfahren kombiniert, zum Beispiel einer Chemotherapie:
- Trastuzumab (Markenname Herceptin®) ist zugelassen als ergänzende Behandlung für Frauen nach der Operation, wenn ihr Befund auf ein höheres Rückfallrisiko hindeutet. Weitere Voraussetzung: Das Tumorgewebe trägt Strukturen, die auf ein aggressives Wachstumsverhalten hindeuten. Gegen diese Strukturen oder “Rezeptoren” richtet sich das Medikament. Trastuzumab erhalten Patientinnen als Infusion.
- Mit Herceptin® wird behandelt, wenn der Tumor bereits Metastasen gebildet hat. Voraussetzung für die Therapie ist auch bei ihnen der Nachweis der Zielstrukturen für den Wirkstoff im Tumorgewebe.
- Lapatinib (Markenname Tyverb®) kann Frauen mit fortgeschrittener Erkrankung und Metastasen helfen. Auch hier ist Voraussetzung, dass der Tumor die entsprechenden Zielstrukturen trägt. Lapatinib kann als Tablette eingenommen werden.
- Bevacizumab (Markenname Avastin®) wird in Deutschland ebenfalls für Frauen mit Metastasen eines Mammakarzinoms eingesetzt, allerdings nur, wenn ihr Tumor nach Einschätzung der Ärzte nicht besser auf andere Mittel anspricht. Bevacizumab ist in Deutschland als Infusionslösung zur Behandlung bei fortgeschrittener Brustkrebserkrankung zugelassen.
- Pertuzumab (Perjeta®) wird nur von Frauen angewendet werden können, deren Erkrankung metastasiert ist und deren Tumorgewebe entsprechende Zielstrukturen für das Mittel aufweist. Siehe auch => Perjeta, Pertuzumab
Psychotherapie
Eine Krebserkrankung ist eine enorme körperliche und seelische Belastung. Ca. 30 Prozent aller an Krebs erkrankten Patienten entwickeln eine psychische Störung. Meistens sind das Depressionen, Angst, Panik, Gedanken an den Tod, akute Belastungsstörungen verursacht durch anstrengende Behandlungen, psychische Störungen verursacht durch veränderte Situation in der Familie, in der Arbeit und durch die allgemeine Leistungsfähigkeit.
Gespräche und Erfahrungsaustausch mit anderen Patienten können hilfreich sein. Besonders wertvoll ist Kontakt zu einer Selbsthilfegruppe. Oft die Unterstützung durch Angehörige und Freunde reicht nicht mehr aus, eine Hilfe von Qualifizierten Ärzten ist sehr empfehlenswert
Siehe auch Seite: => Psychotherapie bei Brustkrebs
Bei der psychoonkologischen Behandlung wird oft Salutogenese angewendet.
Beschreibung der Salutogenese finden Sie hier (im Prostatakrebs Ratgeber): => Salutogenese
Misteltherapie
ist die am häufigsten angewandten Verfahren in der Komplementärmedizin.
Mistel aktiviert Immunsystem, verbessert die Lebensqualität von Tumorpatienten.
Diese Therapie ist mit Vorsicht zu nehmen, da sie auch Allergien verursachen kann, und den Tumorwachstum bei Melanom (schwarzer Hautkrebs) beschleunigen.
Hautentzündung bei Misteltherapie
- Der erwünschte Effekt: Das Brennen, Reizungen, Hautentzündungen der Haut im Bereich der Einstichstelle
- Die Injektionen tun weh und es braucht eine gewisse Überwindung diese sich selber zu machen.
- Für jeder Injektion, wird eine neue Stelle gewählt.
- Die Injektionsstellen können sich infizieren, daraus kann sich die Infektion weiter ausbreiten.
- Auftreten von Fieber
- Mögliche allergische Reaktionen.
Wassersport
Schwimmen und Aquafitness haben für Frauen mit Brustkrebserkrankung besonders große Bedeutung. Durch die Bewegung im Wasser wird das Lymphsystem angeregt, was sehr wichtig ist um ein Lymphödem zu vermeiden.
Gleichzeitig werden die Streßhormone abgebaut und Immunsystem gestärkt.
Brustkrebs: Nachsorge
Früher wurden Patientinnen mit Brustkrebs aufwendige Nachsorgeprogramme mit genau festgelegten Untersuchungsprogrammen empfohlen. Die momentane Darstellung in den Leitlinien ist, dass die regelmäßige Selbstuntersuchung und die klinische Untersuchung durch den betreuenden Arzt anfangs in dreimonatigen, dann in sechsmonatigen, später in einjährigen Abständen ausreichend sind. Labor und apparative Diagnostik werden nur symptomabhängig eingesetzt. Dieser Standpunkt ist jedoch umstritten, da mittlerweile effektive Therapien zur Verfügung stehen, die bei frühzeitiger Erkennung von Metastasierung wesentliche Vorteile im frühen Einsatz bringen könnten.
Patientinnen mit Brustkrebs können vor der Operation zur Einholung einer zweiten Meinung (second opinion) zu uns kommen, sie können nach der Operation zu einer Anschlussheilbehandlung, aber auch zu einer notwendigen Chemotherapie aufgenommen werden.
In ausgewählten Fällen ist es auch möglich, in Kooperation während eines stationären Aufenthaltes bei uns eine Strahlentherapie durchzuführen.